- 83명 대상 임상2상 중간 결과…국내 주요 기관도 참여
- 아미반타맙 단독 경험 환자군 ORR 30%·반응 지속 14.7개월
- 내약성 양호·중증 이상반응 제한적…후속 무료 바카라 게임 공백 제공 기대
[더바이오 성재준 기자] 미국 컬리넌테라퓨틱스(Cullinan Therapeutics)와 일본 타이호제약(Taiho Pharmaceutical)이 공동으로 개발 중인 비소세포폐암(NSCLC) 치료제 후보물질인 ‘지팔러티닙(zipalertinib, 개발코드명 CLN-081, TAS6417)’이 ‘아미반타맙(amivantamab, 상품명 리브리반트)’ 치료 후 진행 환자 대상 임상2b상(REZILIENT1)에서 객관적 반응률(ORR) 30%, 무진행 생존기간(PFS) 7.6개월을 기록하며 효능을 입증했다. 지팔러티닙이 향후 글로벌 승인 과정을 밟을 경우, 무료 바카라 게임(exon20) 변이 NSCLC 환자들에게 새로운 치료 기회를 제공할 수 있을 것으로 기대된다.
이번 연구 결과는 ‘상피세포 성장인자 수용체(EGFR)’ 엑손20 변이 환자에서 후속 치료 대안으로 가능성을 확인한 첫 대규모 분석이다. 해당 결과는 다음달 9일 스페인 바르셀로나에서 열리는 세계폐암학회(WCLC 2025)에서 공식 발표될 예정이다.
또 이번 연구에는 삼성서울병원, 서울아산병원, 국립암센터 등 국내 주요 기관이 참여해 국내 환자들의 임상 결과도 포함됐다. 연구팀은 “이번 결과는 아미반타맙 치료 이후 이어지는 후속 치료 공백을 메울 가능성을 보여준 것으로, 임상적으로 중요한 환자 집단에서 의미 있는 성과”라고 평가했다.
EGFR 엑손20 변이는 전체 폐암 환자의 약 2~4%에서 발견된다. 기존 EGFR 표적치료제에 반응이 낮아 치료가 어려운 변이로 알려져 있다. 현재까지 아미반타맙이 1·2차 치료제로 사용됐지만, 이후 병이 진행하거나 내약성이 떨어진 환자에게는 사실상 치료옵션이 없었다.
REZILIENT1 연구는 아미반타맙 치료 경험이 있는 EGFR 무료 바카라 게임 변이 NSCLC 환자 83명을 대상으로 이뤄졌다. 환자들은 지팔러티닙을 1일 2회(100㎎) 경구 복용했으며, 연령 중앙값은 62세(31~85세), 이전 치료 경험은 평균 2차례였다. 참가자들 중 95%가 항암화학요법을 받았고, 절반 가까이는 면역항암제(anti-PD-(L)1), 40%는 다른 무료 바카라 게임 표적치료제를 사용한 이력이 있었다.
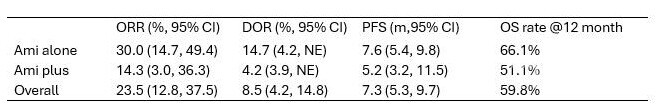
중간 분석 결과, ‘아미반타맙만 사용한 환자군(Ami alone, n=30)’의 ORR은 30%(95% CI: 14.7~49.4), 질병조절률(DCR)은 96.7%였다. 반응 지속기간(DoR) 중앙값은 14.7개월, PFS 중앙값은 7.6개월로 확인됐으며, 12개월 전체 생존기간(OS) 비율은 66.1%에 도달했다.
반면 ‘아미반타맙과 다른 엑손20 표적치료제 경험이 있는 환자군(Ami plus, n=21)’의 ORR은 14.3%(95% CI: 3.0~36.3)에 그쳤다. DoR 중앙값은 4.2개월, PFS는 5.2개월로 낮았으며, 12개월 OS 비율도 51.1%에 머물렀다.
‘전체 환자군(Overall, n=51)’을 합산하면 ORR은 23.5%(95% CI: 12.8~37.5)였다. DoR 중앙값은 8.5개월, PFS는 7.3개월, 12개월 OS 비율은 59.8%로 집계됐다. 연구팀은 “아미반타맙 치료 이후 환자에서도 지팔러티닙이 임상적으로 의미 있는 반응을 보였다”고 설명했다.
지팔러티닙의 안전성은 전반적으로 관리 가능한 수준이었다. 발생률 10%가 넘는 ‘흔한 이상반응’은 조갑주위염(36.1%), 발진(30.1%), 여드름양 피부염(20.5%), 빈혈(20.5%), 구역(16.9%), 피부 건조(15.7%) 등이었다. 3등급 이상 중증 이상반응으로는 빈혈(7.2%), 폐렴·발진·혈소판 감소(각 3.6%)가 보고됐다.
전체 등록 환자 83명 중 용량 감량이나 투여 중단은 각각 7명(8.4%)에서 발생해, 기존 EGFR 표적치료제 대비 비교적 양호한 내약성을 보였다. 연구팀은 “지팔러티닙은 임상적으로 중요한 환자 집단에서 의미 있는 효능과 안전성을 동시에 입증했다”고 평가했다.

