- BMS ‘소틱투’ PsA 적응증 확대 도전…선택적 TYK2 억제제 첫 승인 여부 관심
- ‘레프로잘랍’·‘라이네릭시밧’ 심사 대기…건성안·PBC 소양증 미충족 수요 공략
- 리듬 ‘임시브리’·오차드 ‘marne-cel’ 판정 앞둬…희귀비만·LAD-I 유전자바카라 예측 주목
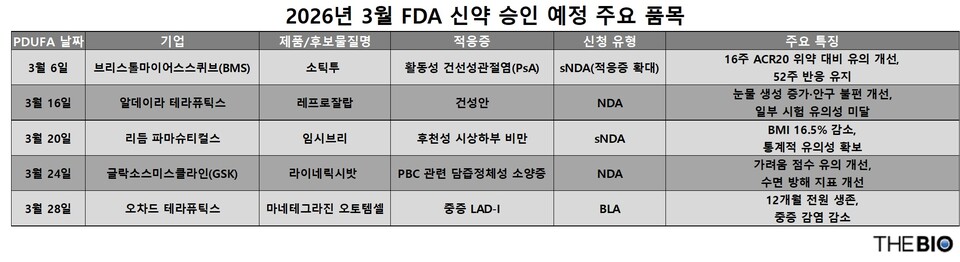
[더바이오 성재준 기자] 미국 식품의약국(FDA)이 3월 한 달간 5개의 주요 신약 또는 신약 후보물질에 대한 승인 여부를 잇달아 결정할 예정이다. 면역·염증질환부터 희귀 비만, 간질환, 소아 유전자치료제까지 다양한 치료 영역이 포함되면서 업계의 관심이 쏠리고 있다.
24일 <더바이오>가 자체 집계한 결과 오는 3월 6일부터 28일까지 총 5건이 처방의약품 사용자 수수료법(PDUFA) 목표일을 맞는다. FDA는 통상 신약 허가 신청(NDA) 또는 생물의약품 허가 신청(BLA) 접수 후 10개월 이내에 승인 여부를 결정하며, ‘우선심사’로 지정될 경우 심사 기간은 6개월로 단축된다.
이번 일정에는 면역·염증, 대사질환, 간질환, 희귀 유전질환 등 다양한 치료 영역의 후보물질이 포함됐다. 승인 여부에 따라 각 질환 영역의 치료옵션 확대 여부가 가려질 전망이다.
◇첫 선택적 TYK2 억제제 도전…‘듀크라바시티닙’ PsA 확대
가장 먼저 3월 6일에는 다국적 제약사 브리스톨마이어스스퀴브(BMS)의 ‘소틱투(Sotyktu, 성분 듀크라바시티닙)’가 활동성 건선성관절염(PsA) 적응증 확대(sNDA)를 두고 FDA 판단을 받는다. 소틱투는 현재 중등도~중증 판상 건선 치료제로 허가돼 있으며, 이번 심사에서는 활동성 PsA 적응증 확대 여부가 쟁점이다.
소틱투는 임상3상(POETYK PsA-1·2) 연구에서 16주차 1차 평가변수인 ACR20 반응률을 위약 대비 유의하게 개선했다. 생물학적 제제 미경험군뿐만 아니라 TNF-α 억제제 치료 경험 환자에서도 일관된 효과를 보였으며, 52주 추적에서도 반응 유지가 확인됐다. 소틱투가 이번에 승인될 경우 PsA 치료 영역 최초의 선택적 TYK2 억제제가 된다.
◇건성안·담즙정체성 소양증…미충족 수요 겨냥
3월 16일에는 미국 바이오기업 알데이라테라퓨틱스(Aldeyra Therapeutics)의 건성안 치료제 후보물질인 ‘레프로잘랍(reproxalap)’이 NDA 심사 결과를 기다리고 있다. 레프로잘랍은 반응성 알데하이드 종(RASP)을 조절하는 저분자 화합물로, 임상3상(TRANQUILITY-2) 등에서 위약 대비 눈물 생성 증가와 안구 불편 개선 효과를 입증했다. 다만 일부 필드 시험에서는 통계적 유의성을 확보하지 못해 심사 결과에 관심이 모인다.
이어 3월 24일에는 원발성 담즙성 담관염(PBC) 환자의 담즙정체성 소양증 치료제 후보물질인 ‘라이네릭시밧(linerixibat)’에 대한 FDA 판단이 예정돼 있다. 다국적 제약사 글락소스미스클라인(GSK)이 개발한 라이네릭시밧은 지난 2023년 10월 공개된 임상3상(GLISTEN) 연구에서 1차 평가변수인 ‘가려움 점수’를 위약 대비 유의하게 개선했으며, 수면 방해 감소 등 주요 2차 지표에서도 통계적으로 의미 있는 개선을 보였다.
◇희귀 비만·소아 면역질환…표적치료 확대
미국 바이오기업 리듬파마슈티컬스(Rhythm Pharmaceuticals)가 개발한 ‘임시브리(Imcivree, 성분 세트멜라노타이드)’도 3월 20일 후천성 시상하부 비만 적응증 확대를 두고 FDA 판단을 받는다. MC4R 작용제인 세트멜라노타이드는 이미 ‘유전성 비만 치료제’로 허가된 약물이다. 세트멜라노타이드는 임상3상(TRANSCEND) 연구에서 위약 대비 체질량지수(BMI)를 16.5% 감소시키며 통계적 유의성을 확보했다. 해당 약이 승인될 경우 시상하부 손상으로 발생하는 희귀 비만 치료 영역에서 새로운 옵션이 추가될 전망이다.
마지막으로 3월 28일에는 미국 바이오기업 오차드테라퓨틱스(Orchard Therapeutics)가 개발한 중증 백혈구부착결핍증-I(LAD-I) 치료제 후보물질인 ‘마네테그라진 오토템셀(marne-cel)’에 대한 BLA 심사 결과가 나올 예정이다. 마네테그라진 오토템셀은 환자의 자가 CD34+ 세포에 ITGB2 유전자를 도입한 조혈모세포 유전자치료제 후보물질이다.
마네테그라진 오토템셀은 임상1·2상에서 12개월 시점 전원 생존을 달성했으며, 추적 기간 중증 감염 발생률 감소와 피부 병변 개선도 확인됐다. 현재 표준치료가 동종 조혈모세포이식에 제한된 만큼, BLA 승인 여부에도 관심이 쏠린다.
