- BMS ‘레블로질’, α 지중해빈혈 2상 성공…수혈 부담 감소 입증
- ‘피루킨드’ 경구 바카라사이트 주사위제 승인…고가·REMS 변수 속 상업화 시험대
- CRISPR 연령 확대·LNP 협업 본격화…유전자바카라사이트 주사위 M&A 재편 가속
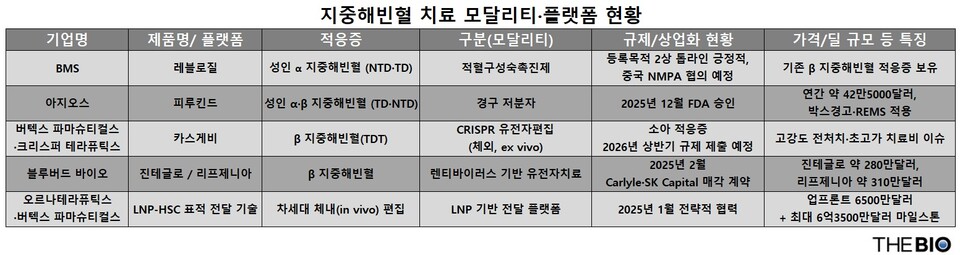
[더바이오 성재준 기자] 평생 반복 수혈이 필요한 유전성 희귀 혈액질환인 ‘지중해빈혈’ 치료 전략이 기존의 ‘수혈 부담 완화’ 중심의 약물 접근을 넘어, 유전자 편집·전달 기술로까지 확장되면서 치료 패러다임을 둘러싼 경쟁 구도도 빠르게 재편되고 있다. 경구용(먹는) 치료제 승인 확대와 적혈구 성숙 촉진제의 적응증 확장, 크리스퍼(CRISPR) 기반 치료의 연령 확대, 지질나노입자(LNP) 전달 플랫폼 협업까지 이어지며 단일 약물 경쟁을 넘어 모달리티와 플랫폼을 아우르는 구도로 치료가 다변화하는 양상이다.
이같은 흐름은 다국적 제약사 브리스톨마이어스스퀴브(BMS)가 23일(현지시간) ‘레블로질(Reblozyl, 성분 루스파터셉트)’의 성인 알파(α) 지중해빈혈 대상 등록 목적 임상2상에서 긍정적인 톱라인(Top-line) 결과를 발표하면서 더욱 선명해졌다. 해당 임상에서 수혈 의존·비의존 환자군 모두 유의미한 개선 효과가 확인됐다. 회사는 관련 데이터를 학회에서 공개하고, 중국 국가약품감독관리국(NMPA) 산하 약품평가센터(CDE)와 허가 절차를 협의할 계획이다.
◇기전 기반 약물 확장…수혈 부담 줄이는 데이터 확보
레블로질은 후기 적혈구 성숙을 촉진하는 계열 내 최초(first-in-class) 바카라사이트 주사위제로, 이번 임상2상에서 수혈 비의존(NTD) 환자군의 13~24주 연속 12주 구간 평균 헤모글로빈(Hb)을 기저치 대비 1g/dL 이상 유의하게 증가시켰다. 수혈 의존(TD) 환자군에서는 13~48주 중 연속 12주 구간에서 적혈구 수혈 부담을 기저치 대비 50% 이상, 최소 2유닛 이상 감소시켰다.
레블로질은 해당 임상에서 모든 주요 2차 평가지표도 충족했다. 기존 베타(β) 지중해빈혈에 국한됐던 적응증을 알파(α) 지중해빈혈로 넓힐 수 있는 근거를 확보했다.
이와 함께 경구용 치료옵션도 상용화 단계에 들어섰다. 미국 바이오기업 아지오스(Agios)의 ‘피루킨드(Pyrukynd, 성분 미타피바트)’는 지난해 12월 미국 식품의약국(FDA)으로부터 수혈 의존성 및 비의존성 알파(α)·베타(β) 지중해빈혈 성인 환자 적응증을 승인받으며, 첫 경구 치료제 지위를 확보했다. 이번 승인은 글로벌 임상3상(ENERGIZE 및 ENERGIZE-T) 연구에서 1차 및 주요 2차 평가지표를 모두 충족한 결과를 기반으로 이뤄졌다.
피루킨드는 수혈 부담 감소와 헤모글로빈 개선, 삶의 질 지표 향상을 입증했다. 다만 일부 환자에서 ‘간세포 손상’을 시사하는 이상반응이 보고되면서 박스 경고와 위험평가 및 완화전략(REMS) 프로그램이 적용됐다. 연간 도매가격은 42만5000달러(약 6억1300만원)로 책정됐다. 상용화 과정에서 안전성 관리와 가격 접근성이 주요 변수로 영향을 미칠 것으로 보인다.
◇CRISPR 유전자 편집 연령 확장…소아 데이터 확보
질환을 근본적으로 교정하는 크리스퍼 기반의 유전자 편집 치료도 확장 국면에 들어섰다. 미국 제약사 버텍스파마슈티컬스(Vertex Pharmaceuticals, 이하 버텍스)와 스위스 크리스퍼테라퓨틱스(CRISPR Therapeutics AG)의 ‘카스게비(CASGEVY, 성분 엑사감글로젠 오토템셀)’는 지난해 12월 미국혈액학회(ASH)에서 5~11세 소아 환자를 대상으로 한 임상 데이터를 처음 공개했다.
수혈 의존성 베타(β) 지중해빈혈 소아 환자 중 충분한 추적 관찰이 가능한 환자 전원이 12개월 이상 수혈이 필요 없는 상태(TI12)를 달성했다. 12세 이상 환자를 포함한 장기 추적 데이터에서도 평균 41개월 이상 수혈 독립이 유지됐다. 회사는 해당 소아 연령군에 대해 올해 상반기 글로벌 규제 제출에 착수할 계획이다.
다만 마이엘로어블레이티브 전처치(골수절제성 전처치)에 따른 독성 위험과 고가 치료비, 장기 안전성 관리 문제는 여전히 한계로 지적된다. 특히 체외(ex vivo) 유전자 편집 치료의 성과가 확인되면서, 다음 단계는 전처치 강도를 낮추거나 체내 전달을 구현하는 기술 경쟁으로 이동하고 있다.
◇유전자 치료 M&A·LNP 협업…전달 플랫폼 경쟁
유전자 치료 상업화를 추진하는 기업들의 구조 재편 움직임도 이어지고 있다. 미국 유전자 치료 전문기업인 블루버드바이오(Bluebird Bio)는 지난해 2월 미국 사모펀드 칼라일(Carlyle)과 미국 사모투자사 SK캐피탈(SK Capital)에 매각되는 계약을 체결했다.
블루버드바이오는 베타(β) 지중해빈혈 치료제인 ‘진테글로(Zynteglo, 성분 자가유래 CD34+ 세포 기반 βA-T87Q-글로빈 유전자)’와 ‘리프제니아(Lyfgenia, 성분 로보티베글로진 오토템셀)’를 비롯한 초고가 단회 투여 유전자 치료제를 보유한 회사로, 높은 약가와 시장 침투 속도에 대한 부담이 이번 거래의 배경으로 지목됐다. 진테글로의 미국 출시가는 약 280만달러(약 40억4000만원), 리프제니아의 경우 약 310만달러(약 44억7200만원) 수준이다.
전달 기술을 둘러싼 플랫폼 경쟁도 본격화됐다. 미국 바이오기업 오르나테라퓨틱스(Orna Therapeutics)는 지난해 1월 버텍스와 전략적인 연구 협력을 체결했다. 계약 규모는 6500만달러(약 938억원)의 업프론트(선급금)와 최대 6억3500만달러(약 9160억원)의 마일스톤(단계별 기술료)으로 구성됐다. 핵심은 조혈모세포(HSC)를 표적하는 LNP 기반의 전달 기술이다.
또 체외(ex vivo) 편집을 넘어 체내(in vivo) 편집으로 확장하려는 흐름이 뚜렷해지고 있다. 이에 따라 편집 효소 자체보다 이를 정확히 표적 조직에 전달하는 플랫폼 기술이 경쟁력의 핵심 요소로 부상하고 있다는 게 업계의 분석이다.
