- ‘엘리비디스’ 3년 추적서 운동 기능 지연 확인…생존·장기 예후 개선은 미확인
- 외부 대조군 기반 장기 데이터 한계…FDA, DMD 유전자바카라 용어 심사에 신중
- 유전자바카라 용어 ‘근본 접근’ 신호에도 엑손 스키핑·저분자 바카라 용어 병존 지속
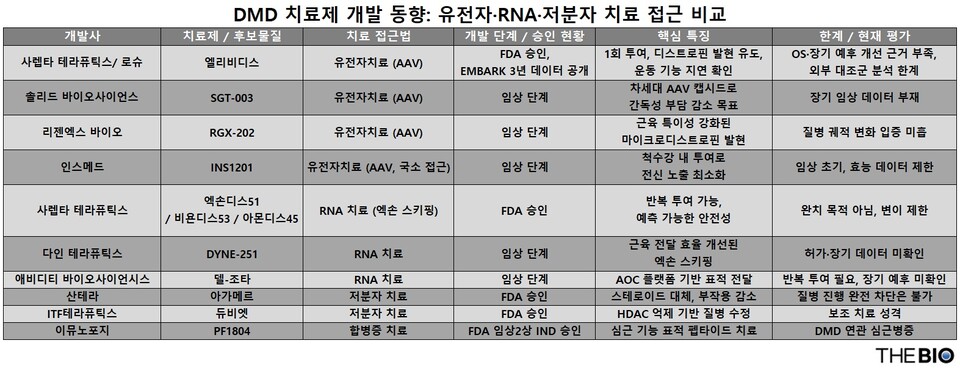
[더바이오 성재준 기자] 희귀 근육질환인 ‘뒤센근이영양증(DMD)’ 치료 영역에서 유전자치료가 질병 진행을 장기간 지연시킬 수 있다는 임상 결과가 공개됐다. 다만 전체 생존기간(OS) 개선이나 장기 예후 변화까지 입증하기에는 근거가 충분하지 않아, 단일 치료 전략이 아닌 다양한 치료 접근이 병존하는 환경은 당분간 이어질 것으로 보인다.
미국 사렙타테라퓨틱스(Sarepta Therapeutics, 이하 사렙타)는 최근 자사의 DMD 유전자치료제인 ‘엘리비디스(Elevidys, 성분 델란디스트로진 목세파보벡)’의 임상3상(EMBARK) 파트1 장기 추적 분석에서 치료 3년 시점까지 질병 진행을 유의하게 지연시키는 효과를 확인했다고 밝혔다. 이번 결과는 ‘보행 가능한 환자’를 대상으로 한 유전자치료의 효능 지속 가능성을 보여주는 데이터로, 연구 내용은 향후 학회 발표와 학술지 게재를 통해 공개될 예정이다.
이번 장기 데이터는 유전자치료가 기존 DMD 치료 접근에서 ‘의미 있는 진전’을 보였음을 보여준다. 다만 생존기간 연장이나 장기 예후 변화를 단정할 수 있는 수준까지는 이르지 않아, 유전자치료와 리보핵산(RNA) 기반 치료가 각기 역할을 나눠 병존하는 치료 환경은 당분간 유지될 것으로 보인다.
◇사렙타, 엘리비디스 3년 데이터서 생존 아닌 ‘기능 유지’ 효과 확인
엘리비디스는 이번 EMBARK 파트1 장기 분석에서 노스스타보행평가(NSAA), 일어서기 시간(TTR), 10미터 보행·달리기(10MWR) 등 주요 운동 기능 지표 전반에서 외부 대조군 대비 통계적으로 유의한 개선 효과를 보였다. 치료 3년 차 기준 엘리비디스 투여군의 NSAA 점수는 베이스라인 이상을 유지한 반면, 외부 대조군에서는 연령 증가에 따른 기능 저하가 관찰됐다. 질병 진행 속도 역시 TTR 기준 73%, 10MWR 기준 70% 지연된 것으로 분석됐다.
다만 이번 결과는 외부 대조군을 활용한 비교 분석이라는 점에서 무작위 대조 임상(RCT) 수준의 확증 데이터로 해석하기에는 한계가 있다. 실제로 이번 분석은 OS 연장이나 호흡·심장 합병증 발생 시점을 늦추는 등 질병의 장기적인 경과 자체가 바뀌었음을 입증한 수준까지는 이르지 않았다.
이는 질환의 자연 경과에서 예측되는 기능 저하 속도를 늦췄다는 점을 보여준 데이터로 해석된다. 즉, 생존을 늘렸다기보다는 보행과 운동 기능을 유지하는 기간을 늘렸다는 의미다.
◇사렙타 개발·로슈 글로벌 상업화…DMD 유전자치료 경쟁은 여전히 제한적
현재 DMD 유전자바카라 용어 시장에서는 엘리비디스를 개발한 사렙타가 유일하게 상업화에 성공한 상황이다. 다국적 제약사 로슈(Roche)는 미국 외 지역에서 해당 바카라 용어제의 상업화를 담당하고 있다.
이밖에 미국 솔리드바이오사이언스(Solid Biosciences)는 차세대 아데노 연관 바이러스(AAV) 캡시드를 적용한 ‘SGT-003(개발코드명)’, 미국 리젠엑스바이오(Regenxbio)는 ‘RGX-202(개발코드명)’, 미국 인스메드(Insmed)는 척수강 내 투여 방식의 ‘INS1201(개발코드명)’을 각각 임상 단계에서 개발 중이다.
이들 기업은 차세대 AAV 캡시드 적용이나 척수강 내 투여 방식 등을 통해 ‘간독성 부담을 낮추는 전략’을 추진하고 있지만, 장기 임상 데이터를 통해 질병 궤적 변화까지 입증한 사례는 아직 나오지 않았다.
DMD 유전자치료 개발에 참여하는 기업 수가 제한적인 배경에는 ‘디스트로핀 유전자’의 구조적인 복잡성과 장기간의 임상 추적이 요구되는 질환 특성, 여기에 안전성 이슈 발생 시 규제 리스크가 급격히 확대되는 환경이 맞물려 있다는 분석이 나온다. 업계에서는 DMD 유전자치료가 질환의 근본 원인을 겨냥한 접근이라는 상징성은 크지만, 단일 표준요법으로 자리 잡기까지는 추가적인 장기 데이터 축적이 불가피할 것으로 보고 있다.
◇RNA·저분자 치료제, DMD 치료의 ‘관리형 축’ 유지
유전자치료와 함께 RNA 기반의 치료제는 여전히 DMD 치료의 한 축을 형성하고 있다. 사렙타가 개발한 ‘엑손디스51(Exondys 51, 성분 에테플리르센)’, ‘비욘디스53(Vyondys 53, 성분 골로디르센)’, ‘아몬디스45(Amondys 45, 성분 카시메르센)’ 등 엑손 스키핑 치료제가 대표적이다.
최근에는 기존 PMO(포스포로디아미데이트 모르폴리노 올리고머) 기반 엑손 스키핑 치료의 한계를 보완하려는 차세대 RNA 치료 접근도 등장하고 있다. 미국 다인테라퓨틱스(Dyne Therapeutics)는 근육 전달 효율을 높인 엑손 스키핑 후보물질인 ‘DYNE-251(개발코드명)’을, 미국 애비디티바이오사이언시스(Avidity Biosciences)는 항체올리고뉴클레오타이드결합체(AOC) 플랫폼 기반의 ‘델-조타(Del-zota, 개발코드명 AOC 1044)’를 각각 임상 단계에서 개발 중이다.
이들 치료제는 특정 유전자 변이를 가진 환자에 한정되지만, ‘반복 투여가 가능’하고 비교적 예측 가능한 안전성 프로파일을 바탕으로 임상 현장에서 활용되고 있다. 유전자치료가 ‘1회 투여’를 통해 질환의 근본적인 해결을 목표로 하는 접근인 반면, RNA 치료는 질병 진행을 억제하며 장기적으로 관리하는 전략으로 병행된다. RNA 치료는 완치를 목표로 하지는 않지만, 질병 진행 속도를 늦추는 ‘관리형 치료 전략’으로 기능하고 있다는 평가다.
이와 함께 스테로이드 대체 약물이나 히스톤 탈아세틸화효소(HDAC) 억제제 등 저분자 ‘질병 수정형 치료제’도 승인되며, DMD 치료옵션은 점차 다변화되고 있다. 스위스 제약사 산테라(Santhera)가 개발한 스테로이드 대체 치료제인 ‘아가메르(Agamree, 성분 바모롤론)’와 미국 ITF테라퓨틱스(ITF Therapeutics)의 HDAC 억제제인 ‘듀비엣(Duvyzat, 성분 기비노스타트)’가 대표적이다. 이들 약물은 완치를 목표로 하지는 않지만, 염증과 섬유화를 조절해 질병 진행을 완화하는 질병 수정형 치료제로 활용되고 있다.
한편, 국내에서는 DMD 자체보다는 합병증을 겨냥한 치료제 개발이 일부 진행되고 있다. 바이오기업 이뮤노포지는 DMD 환자에서 주요 사망 원인으로 꼽히는 ‘심근병증’을 표적으로 한 펩타이드 치료제 후보물질인 ‘PF1804(개발코드명)’를 개발 중이다. 지난해 초 미국 식품의약국(FDA)으로부터 임상2상 시험계획(IND)을 승인받아 임상 개발을 준비하고 있다.

