- 체중 감량·사건 감소·기능적 완치까지…치료 전략 전환 가늠할 대형 바카라 사이트
- 릴리·노바티스·버텍스 등 빅파마 핵심 파이프라인, 상반기 성패 갈린다
- 비만부터 알츠하이머병·유전자치료까지…허가·투자 흐름 좌우할 시험대
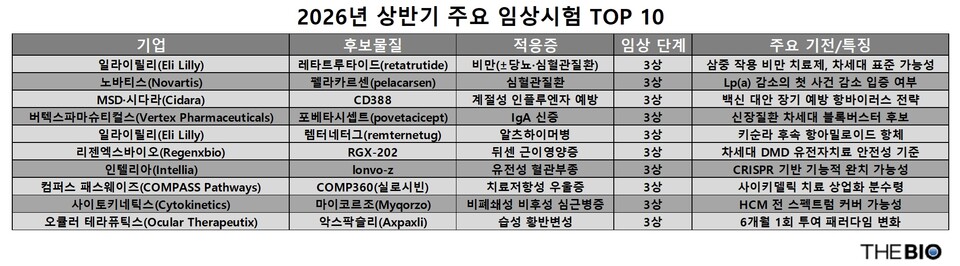
[더바이오 성재준 기자] 올 상반기 글로벌 제약바이오 산업의 향방을 가를 주요 임상시험 결과가 공개될 예정이다. 비만·심혈관·중추신경계(CNS)·유전자치료 분야를 대상으로 한 대형 임상시험 결과가 상반기 중 순차적으로 나온다.
특히 비만·심혈관·CNS·유전자치료 분야는 글로벌 제약사들의 중장기 파이프라인과 직결된 영역이다. 상반기 임상 결과는 단순한 성공과 실패를 넘어, 향후 신약 개발 전략과 투자 방향을 판단하는 참고 지표로 활용될 가능성이 있다.
13일 업계에 따르면, 해당 바카라 사이트시험 결과는 개별 기업을 넘어 관련 치료 영역 전반의 개발 전략과 투자 환경에 영향을 미칠 것으로 예상된다. 글로벌 빅파마와 바이오기업들의 핵심 바카라 사이트이 동시에 진행되는 만큼, 결과에 따라 허가 전략은 물론 인수합병(M&A)과 기술이전(L/O) 기조에도 변화가 나타날 수 있다는 전망이다.
◇비만, 릴리 ‘레타트루타이드’로 삼중 작용 체중 감량 전략 점검
비만 분야에서는 다국적 제약사 일라이릴리(Eli Lilly, 이하 릴리)의 ‘레타트루타이드(retatrutide)’ 임상3상(TRIUMPH-1·2·3) 프로그램이 주요 관전 포인트로 꼽힌다. 레타트루타이드는 글루카곤 유사 펩타이드1(GLP-1), 포도당 의존성 인슐린 분비 촉진 폴리펩타이드(GIP), 글루카곤(GCG)을 동시에 표적하는 삼중 작용기전을 적용한 후보물질로, 기존 GLP-1 계열 치료제 대비 체중 감량 효과의 추가 개선 여부가 이번 임상의 핵심이다.
이번 TRIUMPH 프로그램은 비만 단독 환자뿐만 아니라, 당뇨병 및 심혈관질환을 동반한 환자군까지 포함하도록 설계됐다. 환자 특성별로 체중 감량 효과와 내약성을 동시에 평가한다는 점에서 단일 적응증 중심의 기존 바카라 사이트과는 차별화된 접근으로 평가된다. 업계에서는 해당 결과가 향후 비만 치료제 개발에서 작용기전 다변화와 환자군 세분화 전략에 참고 지표로 활용될 수 있을 것으로 보고 있다.
◇심혈관·신장질환, 노바티스·버텍스 임상 결과 주목
심혈관 영역에서는 노바티스(Novartis)의 ‘펠라카르센(pelacarsen)’ 임상3상(Lp(a) HORIZON)이 핵심 시험으로 꼽힌다. ‘Lp(a)’를 낮추는 것이 실제 심근 경색과 뇌졸중 감소로 이어지는지를 처음으로 검증하는 대규모 사건 기반 임상으로, 결과에 따라 Lp(a) 표적 치료 전략 전반에 영향을 미칠 수 있다는 평가다.
이와 함께 MSD(미국 머크)와 시다라테라퓨틱스(Cidara Therapeutics)가 개발 중인 항바이러스 후보물질인 ‘CD388(개발코드명)’의 임상3상(ANCHOR)도 주목된다. 장기 예방용 항바이러스 전략을 검증하는 시험으로, 기존 백신 중심의 계절성 인플루엔자 예방 접근을 보완할 수 있을지가 관건이다.
신장질환 분야에서는 버텍스파마슈티컬스(Vertex Pharmaceuticals)의 ‘포베타시셉트(povetacicept)’ 임상3상(RAINIER)이 상반기 주요 시험으로 꼽힌다. ‘IgA 신증’을 적응증으로 개발 중인 포베타시셉트는 질환 진행 억제 효과를 평가하는 것이 이번 임상의 핵심으로, 경쟁 약물들이 이미 허가 단계에 진입한 상황에서 차별화된 작용기전과 투여 전략을 통해 치료 환경 내 입지를 확보할 수 있을지 여부가 주목된다.
◇CNS, 알츠하이머병·우울증 주요 임상 결과 주목
CNS 분야에서는 릴리의 알츠하이머병 치료제 후보물질인 ‘렘터네터그(remternetug)’ 임상3상 결과가 상반기 주요 관전 포인트로 꼽힌다. 렘터네터그는 릴리가 2024년 승인받은 항아밀로이드 항체인 ‘키순라(Kisunla, 성분 도나네맙)’ 이후 후속으로 개발 중인 후보물질로, 아밀로이드 제거 효과와 함께 투여 방식의 편의성에서 차별화를 시도하고 있다. 상반기 공개될 임상 결과에서는 초기 알츠하이머병 환자를 대상으로 한 효능과 안전성, 투여 경로에 따른 임상적 유의성이 핵심 평가 지점이 될 전망이다.
이와 함께 컴퍼스패스웨이즈(Compass Pathways)의 ‘실로시빈(psilocybin)’ 기반 치료제 후보물질인 ‘COMP-005·006(개발코드명)’에 대한 임상도 주목된다. 이 연구는 치료 저항성 우울증 환자를 대상으로 한 임상3상 프로그램으로, 단회 투여 후 증상 개선 효과와 지속성을 평가하는 것이 연구의 핵심이다. 해당 임상은 ‘사이키델릭’ 계열 치료제가 제한적 연구 단계를 넘어, 규제 승인과 상업화를 목표로 한 본격적인 개발 단계에 진입할 수 있을지를 가늠하는 시험대가 될 전망이다. 해당 임상 결과에 따라 CNS 치료제 개발 지형에도 일정 부분 영향을 미칠 수 있을 것으로 업계는 보고 있다.
◇유전자치료, 벡터·편집·전달 기술 경쟁 본격화
유전자치료 영역에서는 리젠엑스바이오(Regenxbio)의 뒤센근이영양증(DMD) 치료제 후보물질인 ‘RGX-202(개발코드명)’ 임상3상이 상반기 핵심 시험으로 꼽힌다. RGX-202는 ‘미세디스트로핀(microdystrophin)’ 발현을 목표로 한 유전자치료제 후보물질이다. 이 후보물질은 기존에 승인된 치료제인 ‘엘레비디스(Elevidys, 성분 델란디스트로진 모세파르보벡)’ 이후 강화된 안전성 논의 속에서 차별화된 아데노 연관 바이러스(AAV) 벡터와 단백 발현 전략을 통해 규제당국을 설득할 수 있을지가 핵심 평가 지점이다. 이번 임상 결과는 DMD 유전자치료 분야의 개발 및 허가 기준을 판단하는 참고 자료로 활용될 가능성이 있다.
인텔리아(Intellia)의 크리스퍼(CRISPR) 유전자편집 기술을 기반으로 한 유전성 혈관부종 치료제 후보물질인 ‘lonvo-z’에 대한 임상3상도 중요한 분기점으로 평가된다. ‘단회’ 유전자편집을 통해 질환 증상을 장기간 억제하는 것을 목표로 한 프로그램으로, ‘기능적 완치’ 가능성을 임상적으로 입증할 수 있을지가 핵심이다.
아울러 오큘러테라퓨틱스(Ocular Therapeutix)의 습성 황반변성 치료제 후보물질인 ‘악스팍슬리(Axpaxli)’에 대한 임상3상 역시 주목할 대상이다. 6개월 간격 투여를 목표로 한 지속형 전달 플랫폼 기반 치료제 후보물질로, 기존 항-VEGF 주사제 중심의 치료 부담을 낮출 수 있을지 여부가 상반기 임상 결과의 핵심 평가 지점이 될 전망이다.

