- 美 SABCS 2025서 ‘VRN10’ 임상1상 최신 결과 발표…“초기 용량부터 항종양 효과 확인”
- 240㎎ 투약군까지 3등급 이상 독성 ‘0건’…“현재 320㎎ 용량 증량 투약 진행 중”
[더바이오 유수인 기자] 보로노이는 11일(현지시간) 미국 샌안토니오 유방암 심포지엄(SABCS 2025)에서 인간 상피세포 성장인자 수용체2(HER2)를 표적하는 고형암 치료제 후보물질인 ‘VRN10(개발코드명)’의 임상1상 최신 결과를 발표했다고 밝혔다. SABCS 2025는 지난 9일부터 12일까지 개최된다.
VRN10의 임상1상은 한국과 호주에서 HER2 양성 또는 HER2 돌연변이 고형암 환자를 대상으로 진행 중이다. 이번 발표는 지난 ‘AACR-NCI-EORTC 2025’에서 공개된 80㎎ 및 160㎎ 용량 데이터에 이어 240㎎ 투약군까지의 데이터를 포함했다.
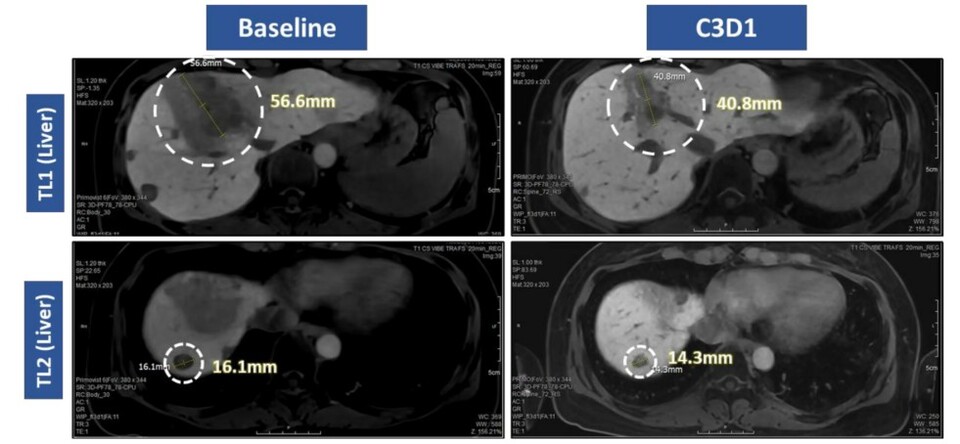
이번 발표에 따르면 VRN10은 초기 용량임에도 불구하고 괄목할 만한 ‘항종양 효과’를 보였다. 80~160㎎까지의 초기 투약군 환자 중 3명에서 종양 감소가 확인됐고, 그중 1명은 종양 크기가 30% 이상 줄어드는 ‘부분관해(PR)’를 달성했다.
특히 ‘엔허투(Enhertu, 성분 트라스투주맙 데룩스테칸)’를 포함한 기존 치료제에 불응하고 종양이 진행된 HER2 변이 유방암 환자에서도 30% 수준의 종양 감소를 보여 폭넓은 치료 가능성을 입증했다고 회사는 강조했다.
뛰어난 효능과 더불어 우수한 안전성도 확인됐다. 현재 240㎎ 용량까지 총 12명의 바카라사이트 신고에게 투약이 진행됐으며, 그중 3등급 이상의 약물 관련 중증 이상반응은 단 1건도 보고되지 않았다.
보로노이는 이러한 결과의 배경으로 VRN10만의 ‘차별화된 약물 기전’을 꼽았다. 이번 학회에서 공개된 비임상 데이터에 따르면, VRN10은 △투카티닙(제품명 투키사, Tukysa) △종거티닙(제품명 헌넥세오스, Hernexeos) △세바버티닙(제품명 하이르누오, Hyrnuo) 등 기존 경쟁 약물들과 달리 HER2의 신호 전달을 억제할 뿐만 아니라, 암세포 표면에 있는 HER2의 내재화(Internalization) 및 분해(degradation)를 유도하는 구조 특이적 기전을 갖고 있다.
이러한 기전적 우월성 덕분에 기존 ‘HER2 티로신 키나아제 억제제(TKI)’ 단독으로는 치료 효과를 기대하기 어려웠던 HER2 돌연변이 암종에서도 효능을 기대할 수 있다는 게 회사의 설명이다. 나아가 엔허투와 같은 항체약물접합체(ADC) 치료제와의 병용 투여 시에도 높은 시너지를 낼 수 있음을 비임상 데이터를 통해 확인했다고 회사는 덧붙였다.
보로노이 관계자는 “현재 320㎎ 용량 증량 투약을 진행 중”이라며 “확보된 약동학(PK) 및 약력학(PD) 분석 결과를 바탕으로 향후 HER2 돌연변이 환자 대상의 ‘단독 임상’은 물론, HER2 양성 고형암 환자를 대상으로 기존 항체치료제 및 ADC와 ‘병용 임상’ 개발을 추진할 계획”이라고 말했다.

